La
Química Orgánica o
Química del carbono es la rama de la
química que estudia una clase numerosa de
moléculas que contienen
carbono formando enlaces covalentes
carbono-carbono o
carbono-hidrógeno, también conocidos como
compuestos orgánicos.
Friedrich Wöhler y
Archibald Scott Couper son conocidos como los "padres" de la química orgánica.
Historia
La química orgánica se constituyó como disciplina en los
años treinta. El desarrollo de nuevos métodos de análisis de las
sustancias de origen animal y vegetal, basados en el empleo de disolventes como el éter o el alcohol, permitió el aislamiento de un gran número de sustancias orgánicas que recibieron el nombre de "principios inmediatos". La aparición de la química orgánica se asocia a menudo al descubrimiento, en
1828, por el químico alemán Friedrich Wöhler, de que la sustancia inorgánica cianato de amonio podía convertirse en urea, una
sustancia orgánica que se encuentra en la orina de muchos animales. Antes de este descubrimiento, los químicos creían que para sintetizar sustancias orgánicas, era necesaria la intervención de lo que llamaban ‘la fuerza vital’, es decir, los organismos vivos. El experimento de Wöhler rompió la barrera entre sustancias orgánicas e inorgánicas. Los químicos modernos consideran compuestos orgánicos a aquellos que contienen carbono e hidrógeno, y otros elementos (que pueden ser uno o más), siendo los más comunes: oxígeno, nitrógeno, azufre y los halógenos.
Un
enlace químico es el
proceso físico responsable de las interacciones atractivas entre
átomos y
moléculas, y que confiere estabilidad a los
compuestos químicos diatómicos y poliatómicos. La explicación de tales fuerzas atractivas es un área compleja que está descrita por las leyes de la
electrodinámica cuántica.
Sin embargo, en la práctica, los químicos suelen apoyarse en la
mecánica cuántica o en descripciones cualitativas que son menos rigurosas, pero más sencillas en su propia descripción del enlace químico. En general, el enlace químico fuerte está asociado con la compartición o transferencia de electrones entre los átomos participantes. Las
moléculas,
cristales, y gases diatómicos -o sea la mayor parte del ambiente físico que nos rodea- está unido por enlaces químicos, que determinan la
estructura de la materia.
Teniendo en cuenta que las cargas opuestas se atraen,porque, al estar unidos, adquieren una situación más estable (de menor
entalpía) que cuando estaban separados. Esta situación de mayor estabilidad suele darse cuando el número de electrones que poseen los átomos en su último nivel es
igual a ocho, estructura que coincide con la de los gases nobles ya que los
electrones que orbitan el núcleo están cargados negativamente, y que los
protones en el núcleo lo están positivamente, la configuración más estable del núcleo y los electrones es una en la que los electrones pasan la mayor parte del tiempo
entre los núcleos, que en otro lugar del espacio. Estos electrones hacen que los núcleos se atraigan mutuamente.
En la visión simplificada del denominado
enlace covalente, uno o más electrones (frecuentemente un
par de electrones) son llevados al espacio entre los dos núcleos atómicos. Ahí, los electrones negativamente cargados son atraídos a las cargas positivas de
ambos núcleos, en vez de sólo su propio núcleo. Esto vence a la repulsión entre los dos núcleos positivamente cargados de los dos átomos, y esta atracción tan grande mantiene a los dos núcleos en una configuración de equilibrio relativamente fija, aunque aún vibrarán en la posición de equilibrio. En resumen, el enlace covalente involucra la compartición de electrones en los que los núcleos positivamente cargados de dos o más átomos atraen simultáneamente a los electrones negativamente cargados que están siendo compartidos. En un
enlace covalente polar, uno o más electrones son compartidos inequitativamente entre dos núcleos.
En una visión simplificada de un
enlace iónico, el electrón de enlace no es compartido, sino que es transferido. En este tipo de enlace, el
orbital atómico más externo de un átomo tiene un lugar libre que permite la adición de uno o más electrones. Estos electrones recientemente agregados ocupan potencialmente un estado de menor energía (más cerca al núcleo debido a la alta
carga nuclear efectiva) de lo que experimentan en un tipo diferente de átomo. En consecuencia, un núcleo ofrece una posición de más fuerte unión a un electrón de lo que lo hace el otro núcleo. Esta transferencia ocasiona que un átomo asuma una carga neta positiva, y que el otro asuma una carga neta negativa. Entonces, el
enlace resulta de la atracción electrostática entre los átomos, y los átomos se constituyen en ((iones)) de carga positiva o negativa.
Todos los enlaces pueden ser explicados por la teoría cuántica, pero, en la práctica, algunas reglas de simplificación les permiten a los químicos predecir la fuerza de enlace, direccionalidad y
polaridad de los enlaces. La
regla del octeto y la (TREPEV) teoría de repulsión de pares de electrones de la
capa de valencia son dos ejemplos. Las teorías más sofisticadas, como la
teoría del enlace de valencia, que incluye la
hibridación de orbitales y la
resonancia, y el método de
combinación lineal de orbitales atómicos dentro de la
teoría de los orbitales moleculares, que incluye a la
teoría del campo de los ligantes. La
electrostática es usada para describir polaridades de enlace y los efectos que ejerce en las sustancias químicas.
Las primeras especulaciones respecto a la naturaleza del
enlace químico son tan tempranas como en el siglo XII, se suponía que ciertos tipos de
especies químicas estaban unidas entre sí por un tipo de
afinidad química. En 1704,
Isaac Newton esbozó su teoría de enlace atómico, en "Query 31" de su
Opticks, donde los
átomos se unen unos a otros por alguna "
fuerza". Específicamente, después de investigar varias teorías populares, en boga en aquel tiempo, de cómo los átomos se podía unir unos a otros, por ejemplo, "átomos enganchados", "átomos pegados unos a otros por reposo", o "unidos por movimientos conspirantes", Newton señaló lo que inferiría posteriormente a partir de su cohesión que:
Las partículas se atraen unas a otras por alguna
fuerza, que en contacto inmediato es excesivamente grande, a distancias pequeñas desempeñan operaciones químicas y su efecto deja de sentirse no lejos de las partículas.
En 1819, a raíz de la invención de la
pila voltaica,
Jöns Jakob Berzelius desarrolló una teoría de combinación química, introduciendo indirectamente el carácter electropositivo y electronegativo de los átomos combinantes. A mediados del siglos XIX,
Edward Frankland, F.A. Kekule, A.S. Couper, A.M. Butlerov y
Hermann Kolbe, ampliando la
teoría de radicales, desarrollaron la
teoría de valencia, originalmente llamado "poder combinante" en que los compuestos se mantenía unidos debido a la atracción entre polos positivo y negativo. En 1916, el químico
Gilbert N. Lewis desarrolló el concepto de
enlace de par de electrones, en el que dos átomos pueden compartir uno y seis electrones, formando el
enlace de un solo electrón,
enlace simple,
enlace doble, o
enlace triple:
En las propias palabras de Lewis:
Un electrón puede formar parte de las envolturas de dos átomos diferentes y no puede decirse que pertenezca a uno simplemente o exclusivamente.
El mismo año,
Walther Kossel lanzó una teoría similar a la de Lewis, con la diferencia de que su modelo asumía una transferencia completa de electrones entre los átomos, con lo que era un modelo de
enlace iónico. Tanto Lewis y Kossel estructuraron sus modelos de enlace a partir de la
regla de Abegg (1904).
En 1927, el físico danés Oyvind Burrau derivó la primera descripción cuántica matemáticamente completa de un enlace químico simple, el producido por un electrón en el ion de hidrógeno molecular (dihidrogenilio), H
2+.
[1] Este trabajo mostró que la aproximación cuántica a los enlaces químicos podrían ser correctas fundamental y cualitativamente, pero los métodos matemáticos usados no podrían extenderse a moléculas que contuvieran más de un electrón. Una aproximación más práctica, aunque menos cuantitativa, fue publicada en el mismo año por
Walter Heitler y
Fritz London. El método de Heitler-London forma la base de lo que ahora se denomina
teoría del enlace de valencia. En 1929,
Sir John Lennard-Jones introdujo el método de
combinación lineal de orbitales atómicos (CLOA o dentro de la
teoría de orbitales moleculares, sugiriendo también métodos para derivar las estructuras electrónicas de moléculas de F
2 (
flúor) y las moléculas de O
2 (
oxígeno), a partir de principios cuánticos básicos. Esta teoría de
orbital molecular representó un enlace covalente como un orbital formado por combinación de los orbitales atómicos de la mecánica cuántica de
Schrödinger que habían sido hipotetizados por los electrones en átomos solitarios. Las ecuaciones para los electrones de enlace en átomos multielectrónicos no podrían ser resueltos con perfección matemática (esto es,
analíticamente), pero las aproximaciones para ellos aún producen muchas predicciones y resultados cualitativos buenos. Muchos cálculos cuantitativos en
química cuántica moderna usan tanto las teorías de orbitales moleculares o de enlace de valencia como punto de partida, aunque una tercera aproximación, la
teoría del funcional de la densidad, se ha estado haciendo más popular en años recientes.
En 1935, H.H. James y A.S. Coolidge llevó a cabo un cálculo sobre la molécula de dihidrógeno que, a diferencia de todos los cálculos previos que usaban funciones sólo de la distancia de los electrones a partir del núcleo atómico, usó funciones que sólo adicionaban explícitamente la distancia entre los dos electrones.
[2] Con 13 parámetros ajustables, ellos obtienen el resultado muy cercano al resultado experimental para la energía de disociación de enlace. Posteriores extensiones usaron hasta 54 parámetros y producen gran concordancia con los experimentos. Este cálculo convenció a la comunidad científica que la teoría cuántica podría concordar con los experimentos. Sin embargo, esta aproximación no tiene relación física con la teoría de enlace de valencia y orbitales moleculares y es difícil de extender a moléculas más grandes.
Teoría de enlace de valencia
En el año 1927, la teoría de enlace de valencia fue formulada, argumentando esencialmente que el enlace químico se forma cuando dos
electrones de valencia, en sus respectivos
orbitales atómicos, trabajan o funcionan para mantener los dos núcleos juntos, en virtud a los efectos de disminución de energía del sistema. En 1931, a partir de esta teoría, el químico
Linus Pauling publicó lo que algunos consideran uno de los más importantes papeles en la historia de la química: "Sobre la naturaleza del enlace químico". En este papel, extendiendo los trabajos de Lewis,la teoría del enlace de valencia (TEV) de Heitler y London, y su propio trabajo previo, presentó seis reglas para el enlace de electrones compartidos, las tres primeras de las cuales generalmente ya eran conocidas:
- 1. El enlace de par de electrones a través de la interacción de un electrón desapareado de cada uno de dos átomos.
- 2. El spin de los electrones tienen que ser opuestos.
- 3. Una vez apareados, los dos electrones no pueden tomar parte en enlaces adicionales.
Sus tres últimas reglas eran nuevas:
- 4. Los términos de canje de electrones para el enlace involucra sólo una función de onda de cada átomo.
- 5. Los electrones disponibles en el menor nivel de energía forman los enlaces más fuertes.
- 6. De dos orbitales en un átomo, el que puede traslapar en mayor cantidad con un orbital de otro átomo formará el enlace más fuerte, y este enlace tenderá a yacer en la dirección del orbital más concentrado.
A partir de este artículo, Pauling publicaría en 1939 un libro de texto: "Sobre la Naturaleza del Enlace Químico" que vendría a ser llamado por algunos como la "biblia" de la química moderna. Este libro ayudó a los químicos experimentales a entender el impacto de la teoría cuántica sobre la química. Sin embargo, la edición posterior de 1939 falló en explicar adecuadamente los problemas que parecían ser mejor entendibles por la teoría de orbitales moleculares. El impacto de la teoría del enlace de valencia declinó durante la década de 1960 y 1970 a la par con el crecimiento en popularidad de la teoría de orbitales moleculares, que estaba siendo implementada en muchos programas de grandes ordenadores. A partir de la década de 1960, los problemas más difíciles de la implementación de la teoría del enlace de valencia en programas de computadoras habían sido mayormente resueltos y la teoría del enlace de valencia vio un resurgimiento.
Teoría de los orbitales formulares

Orbital molecular
HOMO-5 de tipo
pi, en la molécula de trifluoruro de boro, calculado usando Spartan.
La
teoría de los orbitales moleculares (TOM) usa una combinación lineal de
orbitales atómicos para formar orbitales moleculares, que abarcan la molécula entera. Estos orbitales son divididos frecuentemente en
orbitales enlazantes,
orbitales antienlazantes, y
orbitales de no enlace. Un
orbital molecular es simplemente un orbital de Schrödinger que incluye varios, pero frecuentemente sólo dos, núcleos. Si este orbital es del tipo en que los electrones tienen una mayor probabilidad de estar
entre los núcleos que en cualquier otro lugar, el orbital será un orbital enlazante, y tenderá a mantener los núcleos cerca. Si los electrones tienden a estar presentes en un orbital molecular en que pasan la mayor parte del tiempo en cualquier lugar excepto entre los núcleos, el orbital funcionará como un orbital antienlazante, y realmente debilitará el enlace. Los electrones en orbitales no enlazantes tienden a estar en orbitales profundos (cerca a los
orbitales atómicos) asociados casi enteramente o con un núcleo o con otro y entonces pasarán igual tiempo entre los núcleos y no en ese espacio. Estos electrones no contribuyen ni detractan la fuerza del enlace.
Comparación de las teorías del enlace de valencia y de los orbitales moleculares
En algunos aspectos, la teoría del enlace de valencia es superior a la teoría de orbitales moleculares. Cuando se aplica a la molécula más simple de dos electrones, H
2, la teoría del enlace de valencia, incluso al nivel más simple de la aproximación de Heitler-London, produce una aproximación más cercana a la
energía de enlace, y provee una representación más exacta del comportamiento de los electrones al formarse y romperse los enlaces químicos. En contraste, la teoría de orbitales moleculares simple predice que la molécula de hidrógeno se disocia en una superposición lineal de átomos de hidrógeno, y iones positivos y negativos de hidrógeno, un resultado completamente contrario a la evidencia física. Esto explica en parte por qué la curva de energía total versus la distancia interatómica del método de orbitales de valencia yace por encima de la curva del método de orbitales moleculares a todas las distancias y, más particularmente, para distancias mucho más grandes. Esta situación surge para todas las moléculas diatómicas homonucleares y es particularmente un problema para el F
2, para el que la energía mínima de la curva con la teoría de orbitales moleculares es aún mayor en energía que la energía de los dos átomos de flúor no enlazados.
Los conceptos de hibridación son versátiles, y la variabilidad en el enlace en muchos compuestos orgánicos es tan modesta que la teoría del enlace permanece como una parte integral del vocabulario del químico orgánico. Sin embargo, el trabajo de
Friedrich Hund,
Robert Mulliken, y
Gerhard Herzberg mostró que la teoría de orbitales moleculares provee una descripción más apropiada de las propiedades espectroscópicas, magnéticas y de ionización de las moléculas. Las deficiencias de la teoría del enlace se hicieron aparentes cuando las moléculas
hipervalentes (por ejemplo, el PF
5) fueron explicadas sin el uso de los orbitales "d" que eran cruciales en el esquema de enlace basado en hibridación, propuesto para tales moléculas por Pauling. Los
complejos metálicos y
compuestos deficientes en electrones (como el
diborano) también resultaron ser mejor descritos por la teoría de orbitales moleculares, aunque también se han hecho descripciones usando la teoría del enlace de valencia.
En la década de 1930, los dos métodos competían fuertemente hasta que se observó que ambas eran aproximaciones a una teoría mejor. Si se toma la estructura de enlace de valencia simple y se mezcla en todas las estructuras covalentes e iónicas posibles que surgen de un juego particular de orbitales atómicos, se llega a lo que se llama la función de onda de interacción de configuración completa. Si se toma la descripción de orbital molecular simple del estado fundamental y se combina dicha función con las funciones que describen todos los estados excitados posibles usando los orbitales no ocupados que surgen del mismo juego de orbitales atómicos, también se llega a la función de onda de interacción de configuración completa. Puede verse que la aproximación de orbital molecular simple da demasiado peso a las estructuras iónicas, mientras que la aproximación de enlace de valencia simple le da demasiado poco. Esto puede ser descrito diciendo que la aproximación de orbitales moleculares simple es demasiado
deslocalizada, mientras que la aproximación de enlaces de valencia es demasiado
localizado.
Estas dos aproximaciones son ahora observadas como complementarias, cada una proveyendo sus propias perspectivas en el problema del enlace químico. Los cálculos modernos en
química cuántica generalmente empiezan a partir de (pero finalmente van más allá) un orbital molecular en vez de una aproximación de enlace de valencia, no por algún tipo de superioridad intrínseca de la primera, sino porque la aproximación de orbitales moleculares es mucho más rápidamente adaptable a computación numérica. Sin embargo, ahora hay mejores programas de enlace de valencia disponibles.
Enlaces en fórmulas químicas
La tridimensionalidad de los átomos y moléculas hace difícil el uso de una sola técnica para indicar los orbitales y enlaces. En la
fórmula molecular, los enlaces químicos (orbitales enlazantes) entre átomos están indicados por varios métodos diferentes de acuerdo al tipo de discusión. Algunas veces, se desprecian completamente. Por ejemplo, en
química orgánica, la fórmula molecular del etanol (un compuesto en
bebidas alcohólicas) puede ser escrito en papel como
isómeros conformacionales, tridimensional, completamente bidimensional (indicando cada enlace con direcciones no tridimensionales), bidimensional comprimida (CH
3–CH
2–OH), separando el grupo funcional del resto de la molécula (C
2H
5OH), o sus constituyentes atómicos (C
2H
6O), de acuerdo a lo que se esté discutiendo. Algunas veces, incluso se marcan los electrones no enlazantes de la capa de valencia (con las direcciones aproximadas bidimensionalmente,
estructura de Lewis). Algunos químicos pueden también representar los orbitales respectivos.
Enlaces químicos
Longitudes de enlace típicas, en pm,
y energía de enlace en kJ/mol.
Información recopilada de [1]. |
| Enlace | Longitud
(pm) | Energía
(kJ/mol) |
|---|
| H — Hidrógeno |
|---|
| H–H | 74 | 436 |
| H–C | 109 | 413 |
| H–N | 101 | 391 |
| H–O | 96 | 366 |
| H–F | 92 | 568 |
| H–Cl | 127 | 432 |
| H–Br | 141 | 366 |
| C — Carbono |
|---|
| C–H | 109 | 413 |
| C–C | 154 | 348 |
| C=C | 134 | 614 |
| C≡C | 120 | 839 |
| C–N | 147 | 308 |
| C–O | 143 | 360 |
| C–F | 135 | 488 |
| C–Cl | 177 | 330 |
| C–Br | 194 | 288 |
| C–I | 214 | 216 |
| C–S | 182 | 272 |
| N — Nitrógeno |
|---|
| N–H | 101 | 391 |
| N–C | 147 | 308 |
| N–N | 145 | 170 |
| N≡N | 110 | 945 |
| O — Oxígeno |
|---|
| O–H | 96 | 366 |
| O–C | 143 | 360 |
| O–O | 148 | 145 |
| O=O | 121 | 498 |
| F, Cl, Br, I — Halógenos |
|---|
| F–H | 92 | 568 |
| F–F | 142 | 158 |
| F–C | 135 | 488 |
| Cl–H | 127 | 432 |
| Cl–C | 177 | 330 |
| Cl–Cl | 199 | 243 |
| Br–H | 141 | 366 |
| Br–C | 194 | 288 |
| Br–Br | 228 | 193 |
| I–H | 161 | 298 |
| I–C | 214 | 216 |
| I–I | 267 | 151 |
| S — Azufre |
|---|
| C–S | 182 | 253 |
Estos enlaces químicos son fuerzas
intramoleculares, que mantienen a los átomos unidos en las
moléculas. En la visión simplista del enlace localizado, el número de electrones que participan en un enlace (o están localizados en un orbital enlazante), es típicamente un número par de dos, cuatro, o seis, respectivamente. Los números pares son comunes porque las moléculas suelen tener estados energéticos más bajos si los electrones están apareados. Teorías de enlace sustancialmente más avanzadas han mostrado que la
fuerza de enlace no es siempre un número entero, dependiendo de la distribución de los electrones a cada átomo involucrado en un enlace. Por ejemplo, los átomos de carbono en el
benceno están conectados a los vecinos inmediatos con una fuerza aproximada de 1.5, y los dos átomos en el
óxido nítrico, NO, están conectados con aproximadamente 2.5. El
enlace cuádruple también son bien conocidos. El tipo de enlace fuerte depende de la diferencia en
electronegatividad y la distribución de los orbitales electrónicos disponibles a los átomos que se enlazan. A mayor diferencia en electronegatividad, con mayor fuerza será un electrón atraído a un átomo particular involucrado en el enlace, y más propiedades "iónicas" tendrá el enlace ("iónico" significa que los electrones del enlace están compartidos inequitativamente). A menor diferencia de electronegatividad, mayores propiedades covalentes (compartición completa) del enlace.
Los átomos enlazados de esta forma tienen carga eléctrica neutra, por lo que el enlace se puede llamar no polar.
Los enlaces covalentes pueden ser simples cuando se comparte un solo par de electrones, dobles al compartir dos pares de electrones, triples cuando comparten tres tipos de electrones, o cuádruples cuando comparten cuatro tipos de electrones.
Los enlaces covalentes no polares se forman entre átomos iguales, no hay variación en el número de oxidación. Los enlaces covalentes polares se forman con átomos distintos con gran diferencia de electronegatividades. La molécula es eléctricamente neutra, pero no existe simetría entre las cargas eléctricas originando la polaridad, un extremo se caracteriza por ser electropositivo y el otro electronegativo.
Enlace covalente
El enlace covalente polar es intermediado en su carácter entre un enlace covalente y un enlace iónico. Los átomos enlazados de esta forma tienen carga eléctrica neutra.
Los enlaces covalentes pueden ser simples cuando se comparte un solo par de electrones, dobles al compartir dos pares de electrones, triples cuando comparten tres pares de electrones, o cuádruples cuando comparten cuatro pares de electrones.
Los enlaces covalentes no polares se forman entre átomos iguales, no hay variación en el número de oxidación. Los enlaces covalentes polares se forman con átomos distintos con gran diferencia de electronegatividades. La molécula es eléctricamente neutra, pero no existe simetría entre las cargas eléctricas originando la polaridad, un extremo se caracteriza por ser electropositivo y el otro electronegativo.
En otras palabras, el enlace covalente es la unión entre átomos en donde se da un compartimiento de electrones, los átomos que forman este tipo de enlace son de carácter no metálico. Las moléculas que se forman con átomos iguales (mononucleares) presentan un enlace covalente pero en donde la diferencia de electronegatividades es nula.
Se presenta entre los elementos con poca diferencia de electronegatividad (< 1.7), es decir cercanos en la tabla periódica de los elementos quimicos o bien, entre el mismo elemento para formar moleculas diatomicas.
Enlace iónico o Electrovalente
El enlace iónico es un tipo de interacción electrostática entre átomos que tienen una gran diferencia de electronegatividad. No hay un valor preciso que distinga la ionicidad a partir de la diferencia de electronegatividad, pero una diferencia sobre 2.0 suele ser iónica, y una diferencia menor a 1.5 suele ser covalente. En palabras más sencillas, un enlace iónico es aquel en el que los elementos involucrados aceptan o pierden electrones (se da entre un catión y un anión) o dicho de otra forma, es aquel en el que un elemento más electronegativo atrae a los electrones de otro menos electronegativo.
[3] El enlace iónico implica la separación en
iones positivos y negativos. Las cargas iónicas suelen estar entre -3
e a +3
e.
1) Se presenta entre los elementos con gran diferencia de electronegatividad (>1.7), es decir alejados de la tabla periódica: entre metales y no metales. 2) Los compuestos que se forman son solidos cristalinos con puntos de fusión elevados. 3) Se da por
TRANSFERENCIA de electrones: un atomo
PIERDE y el otro '
GANA' 4) Se forman iones
(cationes y aniones)
Enlace covalente coordinado
El enlace covalente coordinado, algunas veces referido como enlace dativo, es un tipo de enlace covalente, en el que los electrones de enlace se originan sólo en uno de los átomos, el donante de pares de electrones, o base de Lewis, pero son compartidos aproximadamente por igual en la formación del enlace covalente. Este concepto está cayendo en desuso a medida que los químicos se pliegan a la teoría de orbitales moleculares. Algunos ejemplos de enlace covalente coordinado existen en
nitronas y el
borazano. El arreglo resultante es diferente de un enlace iónico en que la diferencia de electronegatividad es pequeña, resultando en una covalencia. Se suelen representar por flechas, para diferenciarlos de otros enlaces. La flecha muestra su cabeza dirigida al aceptor de electrones o ácido de Lewis, y la cola a la base de Lewis. Este tipo de enlace se ve en el ion
amonio.
Enlace de uno y tres electrones
Los enlaces con uno o tres electrones pueden encontrarse en especies
radicales, que tienen un número impar de electrones. El ejemplo más simple de un enlace de un electrón se encuentra en el catión de hidrógeno molecular, H
2+. Los enlaces de un electrón suelen tener la mitad de energía de enlace, de un enlace de 2 electrones, y en consecuencia se les llama "medios enlaces". Sin embargo, hay excepciones: en el caso del
dilitio, el enlace es realmente más fuerte para el Li
2+ de un electrón, que para el Li
2 de dos electrones. Esta excepción puede ser explicada en términos de hibridación y efectos de capas internas.
[4]
El ejemplo más simple de enlace de tres electrones puede encontrarse en el catión de helio dimérico, He
2+, y puede ser considerado también medio enlace porque, en términos de orbitales moleculares, el tercer electrón está en un orbital antienlazante que cancela la mitad del enlace formado por los otros dos electrones. Otro ejemplo de una molécula conteniendo un enlace de tres electrones, además de enlaces de dos electrones, es el
óxido nítrico, NO. La molécula de oxígeno, O
2, también puede ser vista como si tuviera dos enlaces de 3-electrones y un enlace de 2-electrones, lo que justifica su
paramagnetismo y su
orden formal de enlace de 2.
[5]
Las moléculas con número impar de electrones suelen ser altamente reactivas. Este tipo de enlace sólo es estable entre átomos con electronegatividades similares.
[5]
Enlaces flexionados
Los [enlaces flexionados], también conocidos como enlaces banana, son enlaces en moléculas tensionadas o impedidas
estéricamente cuyos orbitales de enlaces están forzados en una forma como de banana. Los enlaces flexionados son más susceptibles a las reacciones que los enlaces ordinarios. El enlace flexionado es un tipo de enlace covalente cuya disposición geométrica tiene cierta semejanza con la forma de una banana. doble enlace entre carbonos se forma gracias al traslape de dos orbitales híbridos sp3. Como estos orbitales no se encuentran exactamente uno frente a otro, al hibridarse adquieren la forma de banana
Enlaces 3c-2e y 3c-4e
En el
enlace de tres centros y dos electrones ("3c-2e"), tres átomos comparten dos electrones en un enlace. Este tipo de enlace se presenta en compuestos deficientes en electrones, como el
diborano. Cada enlace de ellos (2 por molécula en el diborano) contiene un par de electrones que conecta a los átomos de boro entre sí, con un átomo de hidrógeno en el medio del enlace, compartiendo los electrones con los átomos de boro.
El
enlace de tres centros y cuatro electrones ("3c-4e") explica el enlace en
moléculas hipervalentes. En ciertos compuestos aglomerados, se ha postulado la existencia de
enlaces de cuatro centros y dos electrones.
En ciertos sistemas conjugados π (pi), como el
benceno y otros compuestos
aromáticos, y en redes conjugadas sólidas como el
grafito, los electrones en el sistema conjugado de enlaces π están dispersos sobre tantos centros nucleares como existan en la molécula o la red.
Enlace aromático
En muchos casos, la ubicación de los electrones no puede ser simplificada a simples líneas (lugar para dos electrones) o puntos (un solo electrón). En
compuestos aromáticos, los enlaces que están en anillos planos de átomos, la
regla de Hückel determina si el anillo de la molécula mostrará estabilidad adicional.
En el
benceno, el compuesto aromático prototípico, 18 electrones de enlace mantiene unidos a 6 átomos de carbono para formar una estructura de anillo plana. El
orden de enlace entre los diferentes átomos de carbono resulta ser idéntico en todos los casos desde el punto de vista químico, con una valor equivalente de aproximadamente 1.5.
En el caso de los aromáticos
heterocíclicos y bencenos sustituidos, las diferencias de electronegatividad entre las diferentes partes del anillo pueden dominar sobre el comportamiento químico de los enlaces aromáticos del anillo, que de otra formar sería equivalente.
Enlace metálico
En un enlace metálico, los electrones de enlace están deslocalizados en una estructura de átomos. En contraste, en los compuestos iónicos, la ubicación de los electrones enlazantes y sus cargas es estática. Debido a la deslocalización o el libre movimiento de los electrones, se tienen las propiedades metálicas de conductividad, ductilidad y dureza.
Enlace intermolecular

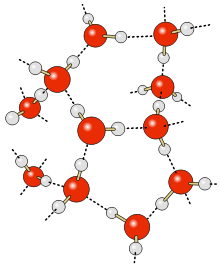
Fuerzas de van der Waals.
Hay cuatro tipos básicos de enlaces que se pueden formar entre dos o más moléculas, iones o átomos que de otro modo no estarían asociados. Las
fuerzas intermoleculares originan que las moléculas se atraigan o repelan unas a otras. Frecuentemente, esto define algunas sus características físicas (como el
punto de fusión) de una sustancia.
Dipolo permanente a dipolo permanente
Una gran diferencia de
electronegatividad entre dos átomos enlazados fuertemente en una molécula ocasiona la formación de un
dipolo (un par positivo-negativo de cargas eléctricas parciales permanentes). Los dipolos se atraen o repelen unos a otros.
Enlace de hidrógeno
En alguna forma este es un ejemplo de un dipolo permanente especialmente fuerte. Sin embargo, en el enlace de hidrógeno, el átomo de hidrógeno está más cerca a ser compartido entre los átomos donante y el receptor, en un
enlace 3-c 2-e. Los enlaces de hidrógeno explican el
punto de ebullición relativamente alto de los líquidos como el agua, amoníaco, y
fluoruro de hidrógeno, comparado con sus contrapartes más pesadas en el mismo grupo de la
tabla periódica.
Dipolo instantáneo a dipolo inducido (van der Waals)
Los dipolos instantáneos a dipolo inducido, o fuerzas de London, son las interacciones más débiles, pero también las más ubicuas, entre
todas las sustancias químicas. Imagine el átomo de helio: en cualquier instante, la
nube electrónica alrededor del átomo (que, de otro modo sería neutral) puede estar ligeramente desbalanceada, con momentáneamente más carga negativa en un lado que en el otro. Esto es a lo que se refiere como un dipolo instantáneo. Este dipolo, con su carga ligeramente desbalanceada, puede atraer o repeler a los electrones en los átomos de helio vecinos, estableciendo otro dipolo (dipolo inducido). Los dos átomos se estarán atrayendo por un instante, antes que la carga se rebalancee y los átomos se muevan.
Interacción catión-pi
La interacción catión-pi se presenta entre la carga negativa localizada de los electrones de un
orbital pi, ubicados sobre y debajo del plano de un
anillo aromático, y una carga positiva.
Electrones en los enlaces químicos
En el límite (irrealístico) del
enlace iónico puro, los electrones están perfectamente localizados en uno de los dos átomos en el enlace. Tales enlaces pueden ser interpretados por la
física clásica. Las fuerzas entre los átomos están caracterizadas por potenciales electrostáticos continuos
isótropos. Su magnitud es una proporción simple a la diferencia de cargas.
Los enlaces covalentes se entiende mejor por la
teoría del enlace de valencia o la
teoría del orbital molecular. Las propiedades de los átomos involucrados pueden ser interpretadas usando conceptos tales como
número de oxidación. La densidad electrónica en el enlace no está asignada a átomos individuales, en vez de ello está deslocalizada entre los átomos. En la teoría del enlace de valencia, los dos electrones en los dos átomos se emparejan con una fuerza de enlace que depende del traslape entre los orbitales. En la teoría del orbital molecular, la
combinación lineal de orbitales atómicos (CLOA) ayuda a describir las estructuras de orbitales moleculares deslocalizados y las energías basadas en los orbitales atómicos de los átomos de los que proviene. A diferencia de los enlaces iónicos puros, los enlaces covalentes pueden tener propiedades de direccionalidad (
anisotropía). Estas pueden tener sus propios nombres, como
sigma y
pi.
En el caso general, los átomos forman enlaces que son intermedios entre iónico y covalente, dependiendo de la
electronegatividad relativa de los átomos involucrados. Este tipo de enlace es llamado algunas veces
enlace covalente polar.
Buckybalón
En 1985, los químicos de la Rice University en Texas utilizaron un láser de alta potencia para vaporizar grafito en un esfuerzo por crear moléculas poco comunes, que se creía existían en el espacio interestelar. La espectrometría de las masas reveló que uno de los productos resultó ser una especie desconocida con la fórmula (C
60). Debido a su tamaño y al hecho de que es carbono puro, esta molécula tiene una forma extraña en la que trabajaron varios investigadores utilizando papel, tijeras y cinta adhesiva. Posteriormente, mediciones espectroscópicas y de rayos X confirmaron que el (C
60) tenían la forma similar a una esfera hueca con un átomo de carbono localizado en cada uno de sus 60 vértices. Geométricamente, el buckybalón (abreviatura de "buckminsterfulerene") es la molécula mas simétrica que se conoce. Sin embargo, a pesar de sus características peculiares, su esquema de enlace es simple. Cada carbono tiene una hibridación sp2, y tiene orbitales moleculares deslocalizados que se extienden sobre la estructura completa. El buckybalón, así como otros miembros de mayor peso representan un concepto completamente nuevo en la arquitectura molecular con implicaciones de largo alcance. Por ejemplo, se ha preparado con un átomo de helio dentro de su estructura. (Chang 440)
Un descubrimiento fascinante, realizado en 1991 por científicos japoneses, fue la identificación de estructuras relacionadas con el buckybalón. Estas moléculas tienen una longitud de cientos de nanómetros y presentan una forma tubular con una cavidad interna aproximada de 15 nanómetros de diámetro. (Chang 440)